Onda-partícula
A las anteriores modificaciones del modelo atómico realizadas a tenor de los descubrimientos experimentales, se sumó un último cambio que afectó a la misma imagen del electrón. Conforme a la noción clásica los electrones eran partículas con masa y carga eléctrica que giraban en órbitas circulares como los planetas del Sistema Solar. Niels Bohr les asignó la capacidad de ganar o perder energía realizando saltos cuánticos entre órbitas. Pero seguían siendo corpúsculos, hasta que el joven físico francés Louis de Broglie propuso la inusual idea de adjudicarles un «comportamiento ondulatorio». La audaz hipótesis intercambiaba los papeles que desempeñaban las partículas y la radiación. El «efecto Compton‛» había puesto de manifiesto que la radiación podía actuar como una partícula y, a la inversa, las partículas podrían comportarse como ondas. Partiendo de esa hipótesis, en 1924, De Broglie defendió con éxito la propuesta de asociar a cada electrón una «onda ficticia» que se extendía a lo largo de la órbita, a modo de una onda estacionaria.
En mecánica, las ondas estacionarias se forman por vibración de una cuerda de longitud L que tiene sus extremos fijos. La mecánica clásica establece que las «longitudes de onda» sólo pueden tener valores múltiplos de la longitud L de la cuerda. Ese resultado justifica así hablar de «longitudes de onda» «cuantizadas», ya que la cuerda vibrará formando longitudes de onda con «determinados» valores enteros. Este resultado que, en principio, sólo expresa una conocida propiedad de la mecánica clásica, fue «transferido idealmente» al modelo atómico. Esta transposición de la física clásica a la física cuántica completaba el modelo del átomo de Bohr.
Con la aportación teórica de De Broglie, los electrones del átomo abandonaban su imagen de partículas que giraban alrededor del núcleo, para convertirse en ondas estacionarias que vibran a lo largo de las órbitas electrónicas. Al principio, la hipótesis, un tanto arriesgada, fue confirmada experimentalmente en 1925 cuando Clinton Davisson, investigador de la Western Electric Company, observó que los cristales producidos por oxidación de una placa de Níquel difractaban un haz de electrones. Y en 1927 se midió el valor de la longitud de onda asociada a los electrones, comprobando que dicho valor coincidía con el predicho por la teoría propugnada por De Broglie.
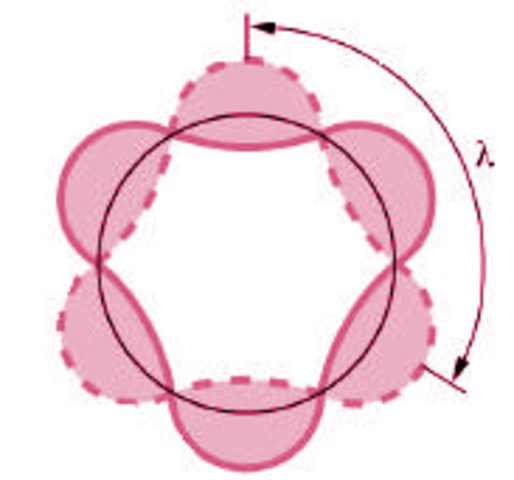
En 1923, De Broglie lanzó la hipótesis de la dualidad onda-corpúsculo. Por lo cual los electrones adquirían esa doble naturaleza. En las órbitas atómicas, los electrones eran considerados como ondas estacionarias.
La construcción del modelo atómico fue un largo proceso desarrollado a lo largo del primer tercio del siglo XX. Comenzó con W. Thomson y siguió con Rutherford, Bohr, Sommerfeld y Pauli, De Broglie. Constituye un ejemplo extraordinario de ingenio y perseverancia, compartida por físicos de diferentes países animados por el mismo esfuerzo intelectual, de descubrir la estructura interna de la materia. Una muestra de colaboración entre la actividad teórica y experimental, que ejemplifica el método científico. Es decir, la construcción paulatina de un «modelo idealizado» a partir de resultados experimentales. Así, el «modelo atómico», no sólo ofrece una explicación de la estructura interna de la materia, sino que además, como recurso intelectual, proporciona el marco conceptual necesario para interpretar nuevos descubrimientos.
Por otra pate, el mismo proceso de construcción del modelo confirma que esa representación no puede considerarse como una especie de radiografía de la realidad material (cualquiera que ésta sea). Más bien, es una composición de piezas que se van encajando dentro del esquema general, pero sin llegar a obtener una imagen completa de la realidad. Las teorías confirmadas por los datos experimentales son válidas, aunque no proporcionen una información completa de las estructuras naturales. Considerado lo expuesto más arriba, no cabe afirmar que, los «entes físicos» construidos (idealmente) para acomodarlos a los datos experimentales, tengan la misma «existencia» real, que los seres materiales que percibimos directamente por los sentidos. Los entes físicos son resultado de idealizaciones, fruto del ingenio y de la experimentación.
Otra consecuencia metodológica que cabe destacar del proceso reseñado en este apartado, se refiere a las características de los conceptos cuánticos. La noción de cuantización se opone a la idea de continuidad. Sin embargo, a partir del concepto cuántico, en «física teórica» se admite una doble identidad asociada a una partícula individual. Así, se asigna al electrón doble naturaleza (ondulatoria y corpuscular). Lo cual contradice los principios de la lógica natural. No obstante, tal «duplicidad de identidad» cumple su función como entidad simbólica, sin referencia o correlación con entidades reales.