El modelo atómico es un ejemplo muy significativo de idealización. Muestra la construcción paso a paso de un esquema ideal en consonancia con los resultados experimentales. A lo largo del proceso de formación, se comprueba la mutua relación entre los descubrimientos experimentales y la teoría. Su comienzo puede datarse hacia 1900, continuando durante los primeros treinta años del siglo XX. En conjunto, fue una empresa científica en la que intervinieron varios investigadores, que aportaron descubrimientos experimentales junto con nuevas hipótesis e interpretaciones teóricas que fueron configurando el modelo atómico.
A) Primer modelo («pudín»)
Hacia el año 1900, William Thomson (Lord Kelvin) (1824 – 1907) ideó un primer esquema, que consistía en una esfera de materia y dotada de carga eléctrica positiva, que contenía pequeños corpúsculos distribuidos (electrones [1]) con carga negativa. En conjunto, esa incipiente versión del átomo ofrecía el aspecto de una masa uniforme donde se alojaban los electrones distribuidos a modo de «pudín».

Modelo ideado por Thomson que se conoce como «pudín». Formado por una distribución de cargas negativas insertadas en una masa homogénea de carga positiva.
B) modelo planetario
En marzo de 1911, Rutherford presentó a la comunidad científica, una segunda versión del modelo el átomo. Se trataba de una esfera en cuyo centro había un núcleo de carga positiva, alrededor del cual giraban electrones siguiendo órbitas circulares concéntricas. La imagen visual ofrecida por este modelo era más compleja que la anterior y dejaba atrás la apariencia estática inicial y adoptando un esquema dinámico análogo al modelo planetario de la mecánica clásica.
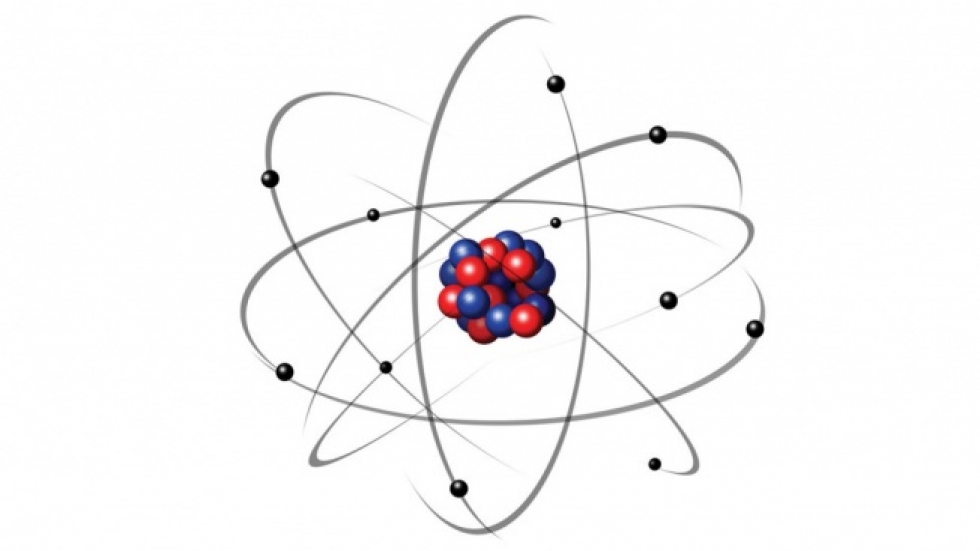
Modelo atómico representando el núcleo en el centro y los electrones girando a su alrededor siguiendo trayectorias circulares.
C) Niveles de energía de Bohr
En 1922, en la revista Zeitschrift für Physik, Bohr publicó una descripción de la estructura de los átomos y de las propiedades físicas y químicas, a partir de la distribución en capas de los electrones de los elementos de la «Tabla Periódica». De acuerdo con los resultados, la nueva versión del modelo atómico tendría una estructura electrónica formada por capas orbitales ocupadas por electrones girando alrededor de un núcleo dotado de carga positiva.
El modelo de Bohr, por su disposición geométrica, era semejante a un sistema planetario. El núcleo ocupa el centro y concentra la mayor cantidad de masa, equivalente al Sol, situado en el centro del sistema solar. Por su parte, los electrones, en forma análoga a los planetas, giran alrededor del núcleo.
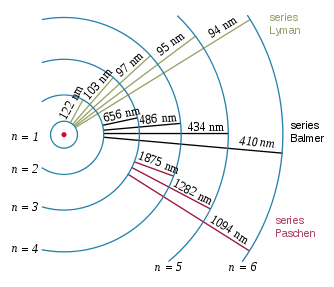
Niveles de energía en el átomo de Bohr, que representan órbitas de electrones. Los saltos a órbitas inferiores suponen pérdida de energía y emisión de radiación de cierta longitud de onda, causa de las rayas espectrales.